Le nouveau règlement européen sur les essais cliniques ne s'applique pas aux vaccins anti-covid déjà sur le marché
- Cet article date de plus de quatre ans.
- Publié le 18 février 2022 à 14:15
- Mis à jour le 18 février 2022 à 16:11
- Lecture : 8 min
- Par : Marie GENRIES, AFP Belgique
"Le nouveau règlement européen relatif aux essais cliniques s’applique à la vaccination Covid", titre cet article du Courrier des Stratèges, un site dont certains articles ont déjà été vérifiés par l'AFP, tout comme certains propos de son fondateur. L'article a été relayé plus de 3 000 fois sur Facebook depuis le 24 janvier, selon l'outil de mesure d'audience Crowdtangle.
"Dans le cadre de la vaccination Covid-19, les vaccins disponibles en France sont en phase 3 d’essais cliniques, jusqu’au 27 octobre 2022 pour Moderna et au 2 mai 2023 pour Pfizer. Jusqu’à ces dates, il s’agit de médicaments expérimentaux utilisés dans un essai clinique", affirme l'autrice de l'article, qui considère donc que le nouveau règlement européen concernant les essais cliniques s'applique à ces vaccins déjà distribués sur le marché.

L'autrice cite notamment une question posée par l'eurodéputée française Michèle Rivasi à la Commission européenne le 7 décembre 2021: "Compte tenu du fait que ces vaccins en phase d’étude clinique sont sous autorisation conditionnelle de mise sur le marché dans l’Union, la Commission peut-elle confirmer que les dispositions du règlement (UE) nº 536/2014 du Parlement européen et du Conseil du 16 avril 2014 relatif aux essais cliniques de médicaments à usage humain (notamment en ce qui concerne le consentement éclairé) restent applicables aux quatre vaccins susmentionnés tant que les essais cliniques se poursuivent, même après une autorisation de mise sur le marché conditionnelle (...) ?".
La réponse - lacunaire - de la Commission européenne, disponible ici, semble être interprétée comme une confirmation par l'autrice de l'article du Courrier des Stratèges, qui conclut que le nouveau règlement européen pourrait donc "être invoqué devant les juridictions nationales" pour protester notamment contre la vaccination obligatoire.
En réalité, ce règlement européen ne s'applique pas aux médicaments déjà sur le marché, ont expliqué à l'AFP la Commission européenne, l'Agence européenne des médicaments (EMA) ainsi que plusieurs experts. Les vaccins, une fois autorisés par l'EMA, ne sont plus considérés par les autorités de santé comme étant en phase d'essais cliniques, bien que les laboratoires continuent à envoyer des données à l'EMA afin de garantir leur sécurité et leur efficacité.
Le principe du consentement éclairé était déjà imposé par la directive précédente
Le règlement UE n°536/2014 relatif aux essais cliniques est entré en vigueur dans l'Union européenne le 31 janvier 2022. Il remplace une directive de 2001, qui encadrait jusqu'à présent les essais cliniques en Europe. Comme l'explique le site de l'UE, le règlement est un acte législatif de portée générale contraignante, tandis que la directive fixe des objectifs aux pays membres, qui sont ensuite tenus de les transposer dans leur droit national.
Ce nouveau règlement "harmonise les procédures de soumission, d'évaluation et de supervision d'essais cliniques de médicaments dans l'UE par le biais du système central d'information sur les essais cliniques" (Clinical Trials Information System, CTIS), explique l'Agence fédérale des médicaments (AFMPS) belge sur son site.
Concrètement, ce nouveau règlement "va simplifier l'approbation de nouveaux essais cliniques", a expliqué à l'AFP Jean-Marie Boeynaems, président du comité d'éthique de l'hôpital Erasme à Bruxelles, interrogé le 15 février 2022. "Avant, si un essai clinique devait avoir lieu dans dix Etats membres, les autorités des dix Etats devaient faire une évaluation séparée du projet. Si sept centres hospitaliers étaient impliqués en Belgique, les sept comités d'éthique devaient donner leur avis. Le nouveau règlement simplifie les choses en désignant un État rapporteur qui va approuver l'autorisation de l'essai clinique".
Si le nouveau règlement européen définit de façon plus précise le consentement éclairé, celui-ci était déjà présent dans la directive de 2001. Comme le précise l'AFMPS dans une autre page dédiée à ce nouveau règlement, les règles sont désormais "harmonisées en ce qui concerne le consentement éclairé, y compris pour la recherche chez les mineurs et chez les sujets frappés d’incapacité".
"Le règlement sur les essais cliniques rationalise la manière dont les essais cliniques sont autorisés et supervisés dans l'UE. Il n'invalide pas, ni ne modifie la façon dont l'EMA considère les résultats des essais cliniques réalisés avant le 31 janvier", a déclaré un porte-parole de la Commission européenne, interrogé le 11 février 2022.
Les vaccins autorisés dans l'UE ne sont pas concernés par le règlement sur les essais cliniques
L'autrice de l'article que nous vérifions évoque des essais cliniques se poursuivant jusqu'en octobre 2022 pour le vaccin de Moderna et jusqu'en 2023 pour le vaccin de Pfizer-BioNTech. Comme expliqué dans un précédent article de vérification, ces dates correspondent à la fin estimée de la collecte des données (efficacité et sûreté à plus long terme) pour la phase III de développement de ces vaccins - le 27 octobre 2022 pour Moderna et le 15 mai 2023 pour Pfizer.
Cependant il est trompeur d'écrire, comme le fait l'autrice de l'article, que "jusqu’à ces dates, il s’agit de médicaments expérimentaux utilisés dans un essai clinique".
Interrogée le 11 février 2022 par l'AFP, une porte-parole de l'Agence européenne des médicaments a expliqué que les vaccins "ont été autorisés sur la base d'une évaluation approfondie de leur qualité, de leur sécurité et de leur efficacité et la conclusion de notre comité scientifique est que leurs bénéfices l'emportent sur leurs risques. Une fois qu'un médicament a reçu une autorisation de mise sur le marché par une autorité réglementaire, il ne peut plus être considéré comme un produit expérimental".
La Commission européenne a également confirmé à l'AFP que le nouveau règlement européen "concerne les essais cliniques et non les vaccins autorisés" par l'EMA. En effet, a indiqué un porte-parole à l'AFP, une fois les vaccins autorisés par l'EMA, les vaccins distribués aux citoyens européens ne sont plus considérés comme expérimentaux ou en phase d'essais cliniques: "La technologie sur laquelle reposent les vaccins dont l'utilisation est autorisée en Europe est en cours de développement depuis plusieurs années. Les vaccins Covid-19 ont été autorisés sur la base d'essais cliniques de très grande envergure, impliquant plusieurs dizaines de milliers de participants pour chaque vaccin".
Comme expliqué à plusieurs reprises par l'AFP dans de précédents articles de vérification (1,2) les vaccins contre le Covid-19 ont fait l'objet d'une autorisation de mise sur le marché (AMM) conditionnelle de l'Agence européenne des médicaments. Cette procédure permet d'autoriser un médicament plus rapidement dans un contexte de situation d'urgence, tout en garantissant sa sécurité.
Actuellement cinq vaccins contre le Covid-19 font l'objet d'une AMM conditionnelle dans l'Union européenne. Il ne s'agit pas d'une nouveauté spécifique au Covid-19: le vaccin Ervebo pour Ebola avait lui aussi reçu une AMM conditionnelle.
Dans le cadre de cette AMM conditionnelle, les laboratoires développant les vaccins peuvent toujours envoyer des données aux autorités compétentes dans les cadre des phases III et IV du développement de ces vaccins, après l'autorisation de mise sur le marché. Comme l'explique la plateforme suisse d'information sur les vaccins Infovac, la phase III inclut des dizaines, voire des centaines de milliers de volontaires.
Si des essais cliniques de phase III sont toujours en cours, c'est parce que "les personnes vaccinées dans le cadre de l'essai clinique continuent d'être suivies pendant 2 ans afin de recueillir davantage d'informations sur la durée de la protection", a expliqué l'EMA à l'AFP. "La phase III, qui est en cours, a également introduit le recrutement de populations supplémentaires, telles que les adolescents et les femmes enceintes, qui ont fourni des données précieuses".
Actuellement, des essais de phase III se poursuivent en parallèle de la mise sur le marché des vaccins, avec les personnes ayant accepté de participer à ces essais. Ce qui ne signifie pas que la population générale vaccinée participe à un essai clinique sans le savoir. Les résultats des essais ont été jugés suffisamment convaincants pour que les autorités sanitaires européennes autorisent les vaccins.
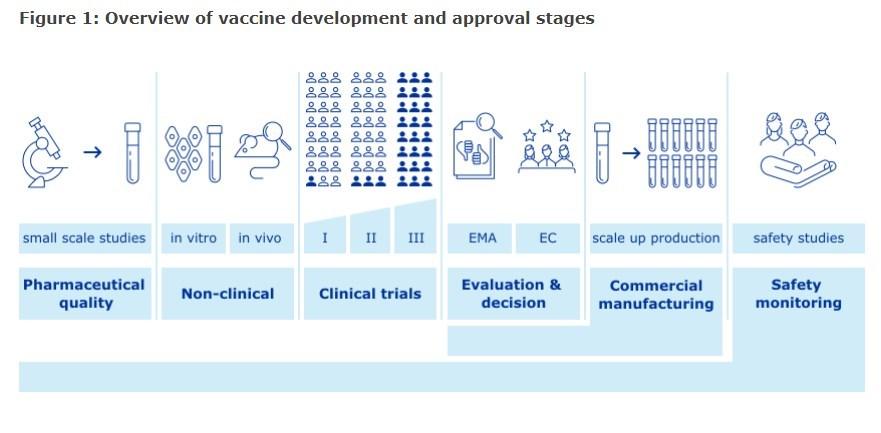
Quant aux essais qualifié "de phase IV", ils sont, indique Infovac, "réalisés après la commercialisation d’un vaccin pour préciser son utilisation auprès de populations qui n’avaient pas été inclues dans les essais de phase II et III. Il s’agit aussi de vérifier si des effets indésirables très rares, mais graves, surviennent chez les millions de personnes vaccinées". L'EMA qualifie cette phase de "contrôle de sécurité" ("safety monitoring").
Ainsi, le laboratoire Pfizer/BioNTech réalise toujours des essais cliniques, comme celui-ci, lancé en mai 2021, qui vise à évaluer la sécurité de son vaccin Comirnaty chez les patients "atteints d'une maladie sous-jacente considérée comme présentant un risque élevé d'aggravation du Covid-19". Dans les critères d'inclusion à cet essai, le laboratoire indique que les participants sont des personnes "capables de comprendre le contenu de cette étude et d'enregistrer leurs symptômes dans un journal d'observation de santé, et qui ont donné leur consentement écrit pour participer à cette enquête (ou leurs parents ou tuteurs légaux dans le cas des mineurs)".
L'argumentation reprise dans l'article que nous vérifions "repose sur une prémisse erronée", a confirmé Jérôme Peigné, professeur en droit de de la santé à l'Université de Paris: "Les vaccins anti-covid qui ont été administrés à la population générale ne sont pas des médicaments expérimentaux, ni au sens de l'ancienne directive ni du nouveau règlement. Ce sont des vaccins qui ont été autorisés par la Commission européenne, c'est-à-dire qu'ils ont l'autorisation d'être commercialisés et utilisés dans tous les Etats membres, par les médecins ou les autres professionnels de santé, notamment dans le cadre d'une campagne de vaccination. Il n'est donc pas exigé un consentement individualisé comme s'il s'agissait d'un essai clinique", a-t-il déclaré le 7 février 2022.
"Depuis qu'il existe une AMM pour ces vaccins, rien n'interdit de faire des essais cliniques post-autorisation. Ils sont même exigés pour confirmer les données de l'AMM ou étendre les indications à des groupes de populations plus jeunes par exemple. Mais ces vaccins ont un statut juridique précis : ce sont des médicaments autorisés. On n'applique la directive et le droit interne ou le règlement du 31 janvier qu'aux essais cliniques, mais pas aux médicaments commercialisés, utilisés, prescrits et administrés au sein de la population générale dès lors qu'ils ont été autorisés", a-t-il poursuivi.
Dès qu'un médicament dispose d'une autorisation de mise sur le marché, quand bien même conditionnelle, "le médicament administré dans ce contexte n'est plus expérimental", a confirmé à l'AFP Julie Vasseur, avocate dans un cabinet dédié aux industries de santé, expliquant qu'"un même médicament peut avoir deux statuts: les vaccins ont le statut de médicament expérimental dans les essais de phase III, mais par ailleurs ils ont reçu une autorisation de l'Agence européenne des médicaments et dans le cadre de cette autorisation, ne sont pas mis sur le marché en tant que médicament expérimental".
"Les autorités réglementaires ont pu récolter suffisamment de données pour garantir un niveau de sécurité élevé des vaccins. Ce n'est pas parce que la phase III se poursuit que les médicaments présentent un danger", a ajouté l'avocate.
"C'est vrai pour tous les médicaments", a ajouté Jean-Marie Boeynaems: "On peut par exemple approuver un médicament, puis celui-ci peut être utilisé dans d'autres essais pour une autre utilisation". Le médecin estime qu'il est "normal qu'il y ait des études réalisées après la mise sur le marché, c'est important car le nombre de personnes qui reçoivent le vaccin est beaucoup plus grand" - et le suivi beaucoup plus précis.
Interrogés à ce propos, tous les experts ont indiqués à l'AFP qu'il était très improbable que ce nouveau règlement européen soit jugé recevable par un tribunal belge ou français dans le cadre d'une contestation de la vaccination obligatoire.
18 février 2022 Fact-check revalidé avec la police d'écriture modifiée dans deux phrases
Copyright AFP 2017-2026. Toute réutilisation commerciale du contenu est sujet à un abonnement. Cliquez ici pour en savoir plus.