Non, la FDA américaine n'a pas interdit des vaccins anti-Covid pour raisons de sécurité
- Cet article date de plus de trois ans.
- Publié le 4 mai 2023 à 14:39
- Lecture : 6 min
- Par : Rob LEVER, Berfin TOPAL, AFP France
"Le gouvernement américain interdit l’utilisation du vaccin Mode[r]na et Pfizer sur le territoire américain", "La FDA n'autorise plus le vaccin nécessaire pour voyager aux États-Unis." De nombreuses publications sur Facebook et Twitter affirment à tort que l’Agence fédérale américaine des produits de santé(FDA) (archive) aurait interdit les vaccins monovalents Pfizer et Moderna.
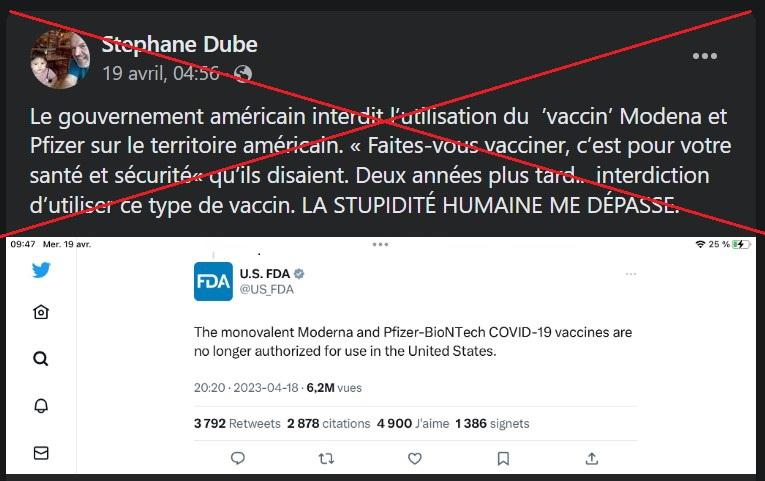
Le 18 avril, la FDA a effectivement mis à jour ses recommandations (archive) sur le vaccin anti-Covid, affirmant que les vaccins monovalents de Pfizer-BioNTech et Moderna ne sont "plus autorisés à être utilisés aux États-Unis".

La FDA a également donné l'information par le biais d'un tweet le 18 avril :
The monovalent Moderna and Pfizer-BioNTech COVID-19 vaccines are no longer authorized for use in the United States.
— U.S. FDA (@US_FDA) April 18, 2023
De façon générale, les vaccins monovalents "immunisent contre un seul agent pathogène" et les vaccins bivalents ou polyvalents "immunisent contre plusieurs sous-types d’un même virus ou d’une bactérie", rappelle (archive) l'Inserm sur son site internet.
Dans le cas du Sars-Cov-2, les monovalents sont les vaccins originaux, contre les premières souches du virus. Les bivalents protègent des variants les plus récents du virus, de la lignée Omicron. Les vaccins bivalents sont "les nouveaux vaccins à ARN messager [...] contre le Sars-CoV-2 et ses variants les plus récents", soulignait fin 2022 le site d'information médicale Vidal le 8 décembre 2022 dans un article (archive).
Reste que la formulation de la FDA sur les vaccins monovalents qui ne seraient "plus autorisés à être utilisés aux États-Unis" est ambiguë.
Une simplification du protocole vaccinal aux Etats-Unis
La tournure du tweet de la FDA a semé une certaine confusion, au point que l'agence a d'ailleurs précisé dans un tweet (archive) en réponse à une question d'Elon Musk, propriétaire de Twitter, que "[...] les vaccins monovalents sont toujours approuvés (ils sont sous licence). Cela n'a pas changé. Mais ils ne sont plus autorisés pour *l'utilisation d'urgence* aux États-Unis."
Comme expliqué dans ce lexique de la terminologie de la FDA (achive), un médicament "approuvé" signifie que l'agence considère que "le médicament est sûr et efficace pour l'usage prévu" et que "les bénéfices du médicament sont supérieurs aux risques quand il est utilisé conformément à sa notice".
Contactée par l'AFP, la FDA confirme que "les affirmations sur les réseaux sociaux selon lesquelles les vaccins monovalents à ARNm COVID-19 ne sont plus autorisés aux États-Unis pour des raisons de sécurité sont entièrement fausses [...]".
La procédure d'"utilisation d'urgence" ("emergency use authorization", EUA) est "un mécanisme visant à faciliter la disponibilité et l'utilisation de mesures médicales, y compris les vaccins, lors d'urgences de santé publique", comme le Covid-19, explique l'agence américaine dans un article (archive) publié fin 2020. La FDA a ainsi pu autoriser l'utilisation de vaccins anti-Covid une fois qu'elle a considéré que les données de sûreté et d'efficacité étaient suffisantes, selon un processus accéléré.
Pour se voir accorder une EUA, le vaccin doit non seulement être sûr et efficace face à une urgence de santé publique mais il faut aussi qu'il n'y ait "pas d'alternatives pertinentes, approuvées et disponibles".
Ces nuances sont aussi expliquées ici dans cet article (archive) de la faculté de médecine de la prestigieuse université américaine de Yale.
Ce qu'a indiqué la FDA le 18 avril, c'est que ce sont désormais les vaccins bivalents qui doivent être utilisés pour immuniser la population car ils sont plus efficaces.
La FDA a expliqué (archive) le 18 avril que les nouvelles directives visent à simplifier le calendrier de vaccination. L'agence recommande désormais une dose unique du vaccin bivalent plutôt que plusieurs doses du vaccin monovalent. C'est en ce sens que les monovalents "ne sont plus autorisés" : ils n'entrent plus dans le cadre de l'EUA.
"La FDA prévoit que la simplification des calendriers de vaccination contribuera à un déploiement plus facile des vaccins, à moins d'erreurs d'administration des vaccins et à une communication moins complexe, autant de facteurs susceptibles d'améliorer les taux de couverture vaccinale et, en fin de compte, d'améliorer la santé publique", a expliqué l'Agence américaine de médicaments à l'AFP.
"Il est désormais prouvé que la majorité de la population américaine âgée de 5 ans et plus possède des anticorps contre le Sars-CoV-2, le virus qui cause le Covid-19, soit par la vaccination, soit par une infection qui peut servir de base à la protection fournie par les vaccins bivalents", explique dans ce même communiqué Peter Marks (archive), directeur du Centre d'évaluation et de recherche en biologie de la FDA (archive).
Claude-Agnès Reynaud (archive), immunologiste et directrice de recherche à l'Institut Necker explique à l'AFP le 25 avril que c'est une manière, pour la FDA, de "simplifier les consignes". Jugeant "raisonnable qu'une consigne de vaccination ne soit qu'une seule chose".
Pas un problème de sécurité
Andrew Pekosz (archive), professeur de microbiologie et d'immunologie à l'Université américaine Johns Hopkins, fait le même constat : les nouvelles directives de la FDA ne sont pas liées à des problèmes de sécurité sur les effets du vaccin. "De nombreuses études chez l'homme ont montré que les profils d'innocuité des formules de vaccins monovalents et bivalents contre le Covid-19 sont presque identiques", explique-t-il à l'AFP le 19 avril.
Olivier Schwartz (archive), directeur de l'unité virus et immunité à l'institut Pasteur précise également le 26 avril à l'AFP que "c'est la séquence de l'ARN qui est modifiée". Il rappelle que ces deux vaccins sont toujours approuvés : "Il n'y a pas eu de remarque nouvelle sur une quelconque toxicité ou des effets secondaires."
Les vaccins bivalents sont mieux adaptés aux variants qui circulent à l'heure actuelle, expliquent les experts contactés à l'AFP. Une explication également soutenue par l'HAS (archive) : "L’efficacité clinique attendue pour ces nouveaux vaccins bivalents est au moins équivalente voire supérieure à celle des vaccins originaux monovalents, sans que cette probable supériorité puisse être actuellement démontrée en vie réelle".
En France, c'est la Haute Autorité de Santé (HAS) (archive) qui régule la mise sur le marché et le protocole concernant les vaccins anti-Covid. Les bivalents sont autorisés depuis septembre 2022.
Selon une note de la Direction Générale de la Santé, du 25 avril 2023 consultée par l'AFP, les deux prochaines campagnes vaccinales françaises se dérouleront au printemps pour les personnes les plus fragiles (pour lesquelles il est "recommandé d’utiliser préférentiellement les vaccins bivalents adaptés à Omicron, quel que soit le vaccin administré précédemment") et une autre à l'automne.
Francesco Salvo (archive), professeur responsable du centre de pharmaco-vigilance de Bordeaux et coordinateur du suivi de la sécurité du vaccin Pfizer, rappelle que la HAS, au 24 février 2023, recommandait déjà le vaccin bivalent en rappel uniquement et pas en première injection. Pour le professeur, ici encore, c'est seulement une question de procédure et non de sécurité. Il explique à l'AFP le 26 avril qu'il est faux de "dire qu'à la première injection, on aura plus de problème avec [le vaccin bivalent] qu'avec les autres" comme le prétendent certains internautes en réaction à la décision de la FDA.
Contacté par l'AFP le 25 avril, le professeur François Chast (archive), pharmacien et ancien chef du service de pharmacie à l'AP-HP, rappelle que "la science s'adapte. Les agences de régulation de la mise sur le marché des médicaments, au fil du renouvellement de l'information scientifique tiennent compte des informations qui leur parviennent". Il explique que ces deux vaccins, monovalent et bivalent, permettent de "minimiser de manière très significative le recours à l'hospitalisation et aux soins intensifs chez les personnes qui ont été vaccinées dans le cadre d'un protocole complet avec une injection initiale et un rappel".
Les autorités de santé publique françaises et mondiales expliquent que les vaccins contre le Covid-19 sont sûrs et efficaces pour prévenir des formes graves de la maladie. Il existe de rares effets secondaires, mais jugés pour une large part d'entre eux légers et temporaires.
La désinformation au sujet des vaccins anti-Covid est massive et récurrente sur les réseaux sociaux, consistant pour l'essentiel à affirmer à tort que les vaccins sont dangereux et/ou que la pandémie n'a pas existé. L'AFP a consacré de très nombreux articles de vérification à ce sujet, qui peuvent être consultés ici.
Copyright AFP 2017-2026. Toute réutilisation commerciale du contenu est sujet à un abonnement. Cliquez ici pour en savoir plus.