Les vaccins anti-Covid adaptés à Omicron "pas testés sur les humains" ? Attention à ces allégations trompeuses
- Cet article date de plus de trois ans.
- Publié le 23 septembre 2022 à 17:02
- Mis à jour le 23 septembre 2022 à 18:36
- Lecture : 13 min
- Par : AFP France
Des vaccins adaptés au variant Omicron qui n'auraient pas été testés lors d'essais cliniques sur des humains avant d'être approuvés par les autorités sanitaires ? C'est ce que prétendent des publications virales sur les réseaux sociaux depuis début septembre.
"Aucune étude humaine n'a été réalisée avant l'approbation des nouveaux 'boosters mis à jour' (...) C'est à la fois sans précédent et imprudent", assure un message vu près de 40.000 fois sur une chaîne Telegram, citant en tant que source un communiqué du "World Council for Health".
Ce dernier est un groupe fondé en 2021 qui remet en question la sécurité des vaccins et promeut des traitements "alternatifs" contre le Covid-19, dont l'efficacité n'a pas été prouvée scientifiquement, et qui a déjà relayé des allégations qui ont fait l'objet de vérifications de l'AFP en anglais.
De nombreux internautes s'inquiètent ou s'alarment dans des messages sur Twitter (1, 2, 3) et sur Facebook à propos de ces vaccins que seraient testés "seulement sur 8 souris", ou recommandés, selon eux, par les autorités sanitaires "sans essais cliniques". Plusieurs personnes nous ont également demandé des précisions au sujet de ces allégations sur WhatsApp.

Des affirmations semblables ont circulé en anglais, alors que les premiers vaccins contre le Covid-19 adaptés au variant Omicron ont commencé à être autorisés à travers le monde.
Elles sont néanmoins trompeuses : les vaccins adaptés au premier sous-variant d'Omicron recommandés en France en septembre 2022 ont bien été testés sur des humains lors d'essais cliniques.
Un vaccin proposé par Pfizer/BioNTech, visant deux autres sous-variants d'Omicron n'a quant à lui été testé que dans une étude pré-clinique sur des rongeurs. Ce dernier vaccin est néanmoins largement similaire aux précédents, et son efficacité attendue et sa sécurité ont donc été estimées suffisantes par les autorités sanitaires. Ce procédé n'est par ailleurs pas inédit : il est aussi utilisé pour les vaccins contre la grippe, virus qui mute rapidement et dont les souches varient sensiblement d'une année à l'autre.
Quels vaccins adaptés à Omicron ?
Comme détaillé dans cet article de l'AFP faisant le point sur les nouveaux vaccins, le virus qui cause la maladie Covid-19, le Sars-CoV-2, mute, et c'est normal. C'est un mécanisme naturel : les virus se multiplient et des modifications génétiques accidentelles peuvent avoir lieu, au gré de la réplication de leur ADN. De façon générale, ces mutations ont permis au Sars-Cov-2 d'être de plus en plus facilement transmissibles.
Les premiers vaccins ont été développés à partir de la souche initiale, dite de Wuhan. Depuis, des variants notables ont émergé, comme Delta ou Omicron. Ce dernier représente précisément une famille de variants, dont plusieurs sous-lignages circulent actuellement, tels BA.1, BA.4 ou BA.5.
Omicron et ses sous-variants ont été dominants tout au long de 2022, prenant rapidement la place des variants précédents. Aujourd'hui, c'est essentiellement le sous-variant BA.5 d'Omicron qui domine en Europe et aux Etats-Unis.
En France, au cours de la semaine du 5 septembre, il représentait 93% des sous-lignages du variant Omicron (le seul variant circulant en métropole à cette date) détectés, selon le site de Santé Publique France.
Pour mieux répondre à ces mutations, les groupes pharmaceutiques adaptent leurs vaccins. Ce fonctionnement n'est pas nouveau : dans le cas de la vaccination contre la grippe par exemple, des vaccins quadrivalents (développés avec des composants de deux souches du type influenza A et de deux virus influenza de type B) sont utilisés.
Dans le cas du Covid, des vaccins dits bivalents sont conçus dans le même but : éduquer le système immunitaire à reconnaître plusieurs attaquants. Les laboratoires Pfizer/BioNTech et Moderna ont ainsi lancé le développement de vaccins, utilisés pour des doses de rappel, qui contiennent à la fois de l'ARN messager (ARNm) du virus original Sars-CoV-2, et de l'ARN messager spécifique au variant Omicron, et à certains de ses sous-lignages.
En France, la Haute autorité de santé (HAS) a ainsi donné le 20 septembre son feu vert à trois de ces vaccins adaptés à Omicron : deux vaccins, l'un de Moderna et l'autre de Pfizer/BioNTech, ciblant la souche originale du virus et le variant BA.1 d'Omicron, et un vaccin de Pfizer/BioNTech ciblant la souche originale et les sous-variants BA.4 et BA.5 d'Omicron.
"Les vaccins à ARNm bivalents ne sont pas des nouveaux vaccins mais des vaccins adaptés aux souches circulantes, à l'instar des vaccins contre la grippe saisonnière dont l'actualisation annuelle tient compte des virus qui sont le plus susceptibles de circuler pendant l'hiver, selon les préconisations de l'OMS", note la HAS dans son avis.
Les vaccins visant le sous-variant BA.1, bien testés sur des humains
Les premiers vaccins, adaptés au sous-variant BA.1 d'Omicron, ont bien fait l'objet de tests sur les humains, comme l'indiquent les agences du médicament américaine, européenne, ainsi que la Haute autorité de santé (HAS) dans leurs avis respectifs.
Concernant le vaccin de Pfizer/BioNTech ("Comirnaty Original/Omicron BA.1"), l'Agence européenne des médicaments (EMA) notait le 1er septembre que sa recommandation était fondée sur "deux études", qui ont mesuré et comparé les anticorps chez des personnes ayant reçu le vaccin original et le vaccin adapté à Omicron.
La première, menée sur "des adultes de 55 ans et plus ayant précédemment reçu trois doses de Comirnaty", a inclus "plus de 1.8000 personnes, parmi lesquels 300 ont reçu Comirnaty Original/Omicron BA.1", le vaccin bivalent. Selon l'avis de l'EMA, elle "a montré que la réponse immunitaire au sous-variant BA.1 d'Omicron était plus importante après une deuxième dose de Comirnaty Original/Omicron BA.1 qu'après une dose du vaccin original Comirnaty (d'après les mesures d'anticorps visant le sous-variant Omicron BA.1)".
La deuxième étude, menée sur "plus de 600 personnes entre 18 et 55 ans", a également "montré que la réponse immunitaire au sous-variant BA.1 d'Omicron était plus élevée chez les personnes ayant reçu un rappel avec un vaccin contenant seulement le composant visant Omicron BA.1 que chez celles ayant reçu un rappel avec le vaccin Comirnaty original".
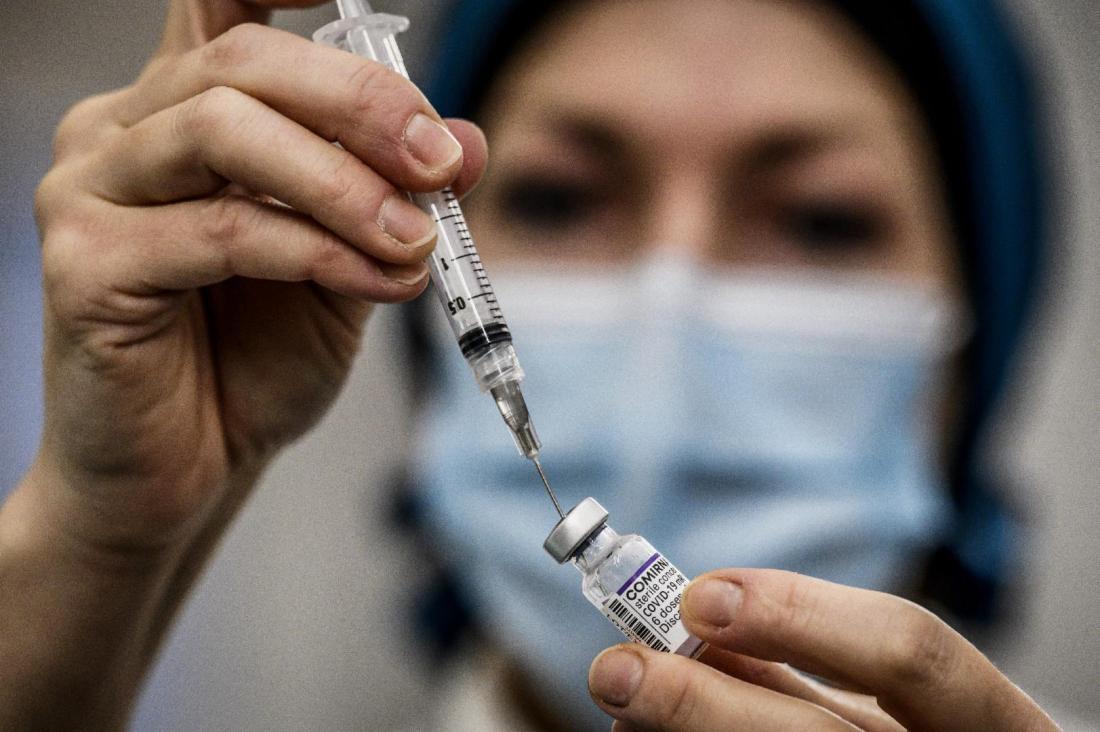
Concernant le vaccin de Moderna ("Spikevax bivalent Original/Omicron BA.1"), la recommandation de l'EMA a été fondée sur "les données d'une étude impliquant plus de 800 adultes âgés de 18 ans et plus".
"Les conclusions de l'étude ont montré qu'un rappel de Spikevax bivalent Original/Omicron BA.1 a induit une réponse immunitaire plus importante contre le Sars-CoV-2 et contre le sous-variant d'Omicron BA.1, en comparaison d'un rappel de Spikevax original", indique l'avis de l'EMA.
"Ce qui a été testé, c'est l'immunogénicité [la capacité à induire une réaction immunitaire, NDLR] de ces vaccins. Avec le mélange avec Omicron, il y a un petit gain du nombre d'anticorps, de facteur deux, ce qui n'est pas énorme, mais permet de gagner de la protection dans le temps", détaille Olivier Schwartz, directeur de l'unité virus et immunité à l'Institut Pasteur, le 23 septembre à l'AFP.
Ces deux vaccins ont été autorisés dans l'Union européenne le 1er septembre, à la suite de l'avis positif de l'EMA. "Des essais cliniques ont été menés, et ont montré que les nouveaux vaccins adaptés [au sous-variant BA. 1 d'Omicron, NDLR] permettent de développer une quantité supérieure d'anticorps capables de neutraliser le variant Omicron BA.1, par rapport aux actuels vaccins monovalents actuels basés sur la souche originale", résume l'EMA dans un communiqué publié le 8 septembre.
"Les effets secondaires observés avec ces vaccins adaptés étaient comparables à ceux observés avec les vaccins originaux, et étaient généralement légers et de courte durée", note encore l'EMA.
Dès le 15 août, le régulateur britannique du médicament avait approuvé le vaccin de Moderna adapté à Omicron.
Le 31 août, la FDA, agence américaine des médicaments, avait annoncé autoriser ces vaccins de Pfizer/BioNTech et Moderna, en s'appuyant sur des "études cliniques", ainsi qu'un troisième, visant les sous-variants BA.4 et BA.5, qui sont, en septembre 2022, majoritaires aux Etats-Unis et en Europe.
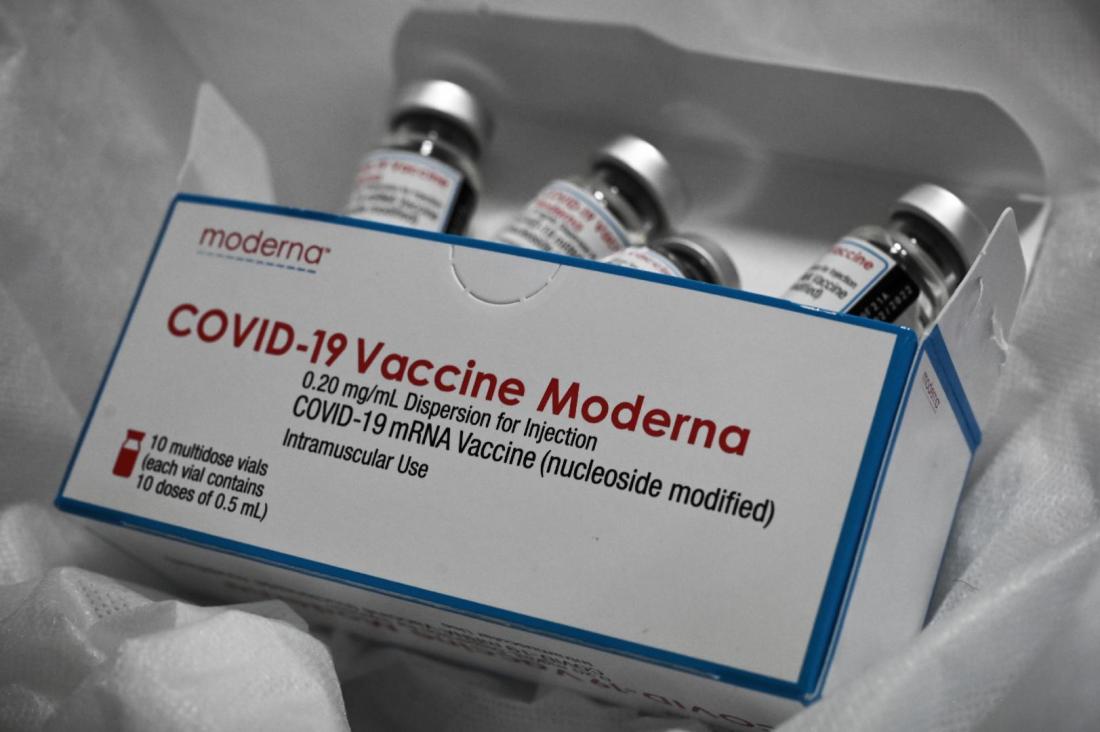
Une composition très proche pour le vaccin visant les sous-variants BA.4-5, en cours de tests
Ce troisième vaccin a aussi été autorisé le 12 septembre par l'Agence européenne du médicament. Une semaine plus tard, la HAS l'a aussi recommandé en France, avec les deux premiers visant le sous-variant BA.1.
Les essais cliniques visant à tester ce troisième vaccin, adapté à des sous-variants apparus plus tardivement, sont toujours en cours. Ainsi, l'avis de la HAS "repose essentiellement sur une étude préclinique chez les souris, et deux études cliniques", qui ont pris en compte le vaccin adapté au sous-variant BA.1.
"Cette procédure d'évaluation, basée sur des données plus limitées que lors d'une évaluation initiale, permet d'assurer la mise à disposition très rapide des vaccins les plus adaptés au contexte épidémiologique et à la souche circulante. Elle se justifie d'une part par le recul important (sur le plan de l'efficacité et de la tolérance) acquis depuis le début de la crise sanitaire concernant les vaccins à ARNm, et également par l'expérience acquise en vaccinologie concernant les vaccins adaptés aux souches nouvellement circulantes (exemple de la grippe saisonnière et données obtenues avec le vaccin bivalent BA.1 par rapport au vaccin original", détaille la HAS.
Dans sa recommandation, l'EMA estimait aussi que "mis à part le fait qu'ils contiennent des séquences d'ARNm des sous-variants d'Omicron légèrement différentes, mais néanmoins très proches, 'Comirnaty Original/Omicron BA.4-5' et 'Comirnaty Original/Omicron BA.1' ont la même composition".
Ce que Marco Cavaleri, le responsable de la stratégie vaccinale de l'EMA, a détaillé le 20 septembre lors d'un point sur le Covid-19. "Il est important de comprendre que les données cliniques concernant un vaccin adapté [à un sous-variant, NDLR] aident à l'évaluation d'autres vaccins adaptés [à d'autres sous-variant, NDLR], particulièrement lorsque les différences de composition sont aussi mineures qu'entre 'Comirnaty bivalent Original/Omicron BA.1' et 'Comirnaty bivalent Original/Omicron BA.4-5', qui ont essentiellement la même composition. Ce qui les rend différents, c'est qu'ils contiennent des des séquences d'ARNm des sous-variants d'Omicron légèrement différentes, mais très proches, avec seulement une différence dans le codage de quelques acides aminés", a-t-il expliqué.
"Extrapoler les résultats d'un vaccin à un autre est une approche scientifiquement établie et documentée, qui se fonde sur des concepts d'immunologie largement acceptés", a-t-il aussi ajouté, soulignant que ce fonctionnement est "semblable" à celui utilisé pour les vaccins anti-grippe, et que l'avis de l'EMA concernant ce vaccin "s'appuie sur les connaissances larges acquises lors du déploiement des vaccins originaux contre le Covid-19, avec des milliards de doses administrées dans le monde".
L'avis de la FDA aux Etats-Unis était également parvenu aux mêmes conclusions fin août. "Ce que nous faisons ici est ce que nous faisons chaque année pour le vaccin contre la grippe", abondait alors Peter Marks, le directeur du centre d'évaluation biologique et de recherche de la FDA.
"L'espoir" avec ce vaccin est de "restaurer" un niveau d'immunité similaire à celle conférée par les vaccins au moment où ils avaient été lancés, et de procurer une "durée de protection plus longue", afin de ne pas avoir à répéter les rappels trop souvent, estimait aussi Peter Marks.
Dans une présentation en juin 2022, la FDA avait mis en avant des premières données fondées sur des recherches comparant l'immunogénicité des vaccins chez dans trois groupes de huit souris, ayant reçu des vaccins originaux seuls ou combinés avec des versions visant Omicron. Ces premières données montraient une meilleure réponse immunitaire des souris ayant reçu des vaccins combinés. C'est de cette dernière que semble avoir émergé le chiffre de "huit souris" circulant sur les réseaux sociaux.
Interrogée au sujet de ces vaccins dont les essais cliniques sont toujours en cours, Emmanuelle Blanc, directrice médicale de l'activité vaccins chez Pfizer, assure le 22 septembre lors d'un point presse qu'"on ne part pas de rien en terme de tests chez l'humain", puisque depuis le début de la pandémie, plusieurs vaccins bivalents ont été développés par l'entreprise.
"On a développé un bivalent Alpha/Delta au moment où il y avait la vague Delta, qui est passée mais on a quand même les données de sécurité. Ces vaccins bivalents, que ce soit Alpha/Delta, Original/Beta, Original/BA.1, Original/BA.4.5, ils ont tous la même quantité d'ARN messager. Il y a juste la séquence de la protéine 'Spike' qui varie. C'est la même structure, les mêmes particules nano-lipidiques qui encapsulent le vaccin, c'est la même formulation. On a toutes ces données cliniques de sécurité, de tolérance qui ont été soumises aux autorités réglementaires. L'étude est en cours mais on sait qu'on peut comparer ces différentes versions de notre vaccin, et que toutes les données de sécurité sont très cohérentes et très constantes par rapport à toutes ces 'versions' de notre vaccin", abonde-t-elle.
Pour la HAS, contactée par l'AFP le 21 septembre, il est donc "réducteur" d'affirmer que le vaccin adapté à Omicron n'a été testé "que sur des souris".
Une procédure déjà utilisée pour les vaccins anti-grippaux
Le processus de développement de ces vaccins n'est par ailleurs pas totalement inédit, puisqu'ils ont été développés d'une façon semblable aux vaccins anti-grippaux, ont souligné un spécialiste en épidémiologie, un virologue et une immunologiste auprès de l'AFP.
"Le développement de ces nouveaux vaccins bivalents du Covid a été conduit selon le modèle courant des vaccins saisonniers contre la grippe. La composition des vaccins contre la grippe varie d'une année sur l'autre et les fabricants n'ont ni le temps ni la possibilité matérielle d'en évaluer leur efficacité par des essais cliniques, car la grippe est saisonnière et ne produit qu'une vague par saison froide", détaille le directeur de l'Institut de santé mondiale de l'université de Genève et spécialiste en santé publique et en épidémiologie Antoine Flahault le 21 septembre à l'AFP.
"Dans le cas des vaccins du Covid, on est dans une configuration différente puisque les fabricants auraient pu conduire des essais cliniques évaluant leur efficacité préalablement à leur enregistrement. Mais cela aurait évidemment retardé la soumission de leur dossier aux agences de sécurité sanitaire et les vaccins n'auraient pas pu être prêts dès l'automne. Les fabricants ont ainsi négocié directement avec les autorités pour obtenir un statut d’enregistrement voisin de celui des vaccins contre la grippe", abonde-t-il.
L'immunologiste et directrice de recherche à l'Institut Necker Enfants Malades Claude-Agnès Reynaud, complète : "on est dans la nouveauté, il n'y a aucun doute. Mais c'est un fonctionnement totalement logique qui permet de gagner du temps, et c'est le but des vaccins à ARNm de pouvoir s'adapter face aux variants du virus. En faisant un essai clinique, on aurait le résultat dans six mois. D'ici là, un autre variant sera peut-être là".
"Le premier vaccin qui vise BA.1 a bien été testé sur des humains. Après, on entre dans une logique d'adaptation au variant, où on peut remplacer le BA.1 par n'importe quoi de très proche, comme le BA.4, le BA.5... Ce sont des petites séquences de la protéine 'Spike' qui changent entre les variants", explique-t-elle encore.
"A mes yeux, il n'y a pas lieu de s'inquiéter, c'est la même composition à l'exception de cette petite portion d'ARNm qui correspond au BA.1", résume aussi Olivier Schwartz de l'Institut Pasteur.
Lorsque le vaccin avait été approuvé aux Etats-Unis, certains experts avaient toutefois émis des interrogations sur l'étendue de l'efficacité renforcée que ces vaccins actualisés pourraient apporter, celle-ci ne pouvant être mesurée que via des essais cliniques.
"Les agences auraient pu exiger des essais cliniques, mais ont préféré aller vite, en prenant un pari risqué pour le capital confiance du public s'il s'avérait que ces vaccins étaient moins efficaces que les monovalents, ce qui est certes peu probable mais que l'on n'a pas vérifié à présent", souligne pour sa part auprès de l'AFP Antoine Flahault le 23 septembre.

L'importance des données de pharmacovigilance
Dans leurs recommandations, les agences des médicaments européenne et américaine ainsi que la HAS notent que leurs avis pourront être mis à jour en fonction de l'arrivée des nouvelles données.
Tous les spécialistes interrogés par l'AFP soulignent aussi l'intérêt de la pharmacovigilance, qui permet notamment de récolter des données sur les potentiels effets indésirables des vaccins. "La pharmacovigilance est importante, elle nous fait avancer. Aujourd'hui, on est tout le temps dans l'observation", note Claude-Agnès Reynaud.
Marco Cavaleri de l'EMA indiquait aussi dans son point du 20 septembre qu'"il sera important de recueillir des données sur les performances des nouveaux vaccins dans la vie réelle, afin de comprendre jusqu'où ils protègent des personnes contre l'infection et les maladies graves en automne et en hiver, et la durée de cette protection".
Depuis le début de la pandémie de Covid-19, de nombreuses publications trompeuses ou fausses au sujet des vaccins circulent. L'AFP a réalisé plus de 790 articles de vérification en français liés au Covid-19 depuis le début de la pandémie, au 23 septembre 2022.
23 septembre 2022 Ajoute citation d'Antoine Flahault
Copyright AFP 2017-2026. Toute réutilisation commerciale du contenu est sujet à un abonnement. Cliquez ici pour en savoir plus.